dir="rtl">
التحول الإشعاعي: تغير عنصر إلى عنصر آخر بفقد جسيمات (ألفا، بيتا) وطاقة من نواة غير مستقرة.
جسيمات ألفا (α): نواة الهيليوم (2 بروتون، 2 نيوترون). تفقدها النواة فيقل العدد الذري بمقدار 2 والكتلي بمقدار 4.
جسيمات بيتا (β): إلكترونات عالية الطاقة تنبعث من النواة نتيجة تحول نيوترون إلى بروتون، فيزيد العدد الذري بمقدار 1.
كاشف الدخان: يستخدم عنصر أمريكيوم-241 لإنتاج جسيمات ألفا. دخان الحريق يعطل التيار فيشغل الإنذار.
استخدامات النظائر المشعة: في الطب (التشخيص، علاج السرطان)، الزراعة (تتبع الأسمدة، مكافحة الآفات)، الصناعة.
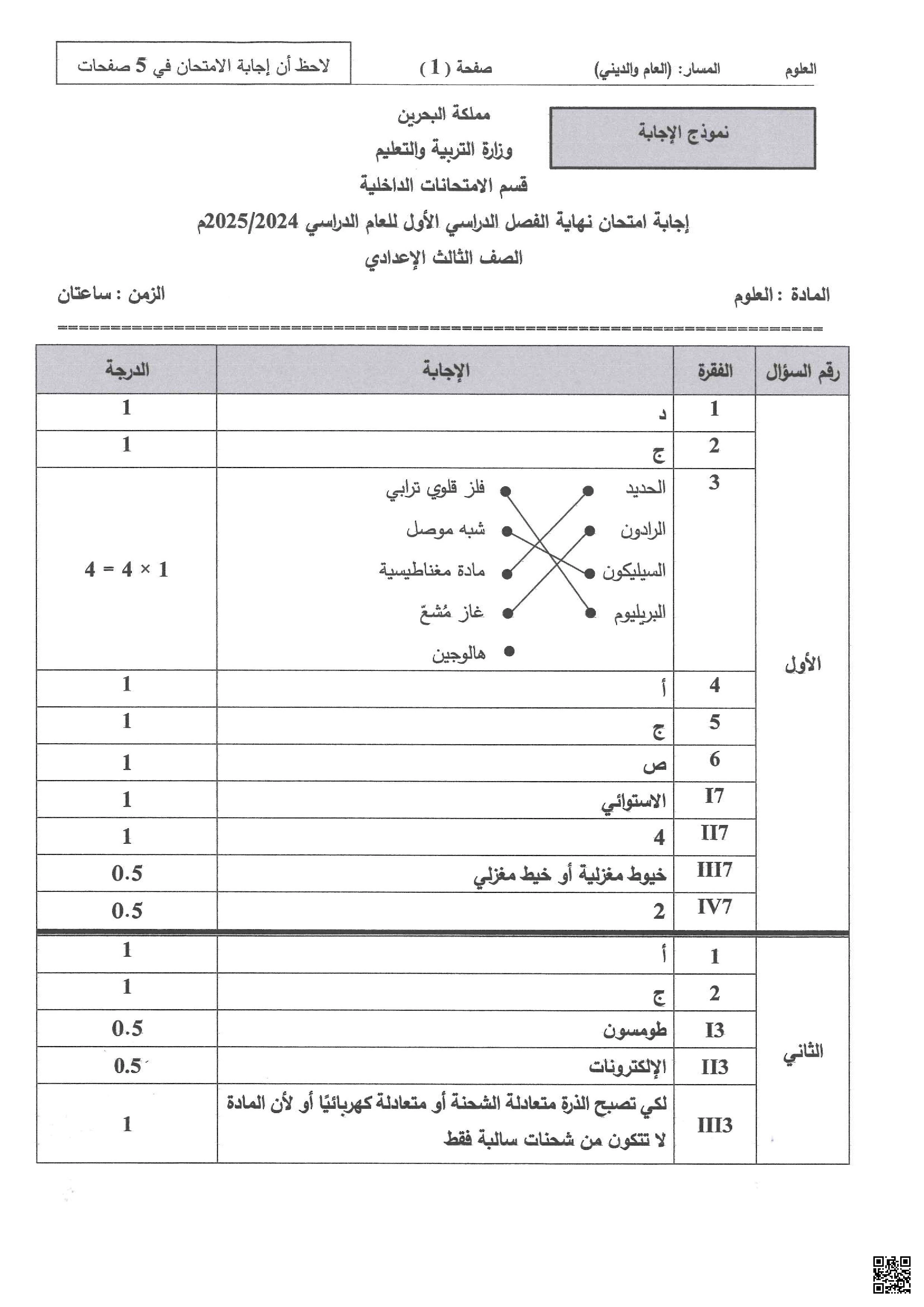
الجدول الدوري: رتبه موزلي حسب العدد الذري. يحتوي على 18 مجموعة و7 دورات.
الفلزات: يسار/وسط الجدول، صلبة (عدا الزئبق)، لامعة، موصلة، قابلة للطرق والسحب.
اللافلزات: يمين الجدول، غازية أو هشة، باهتة، رديئة التوصيل.
أشباه الفلزات: بين الفلزات واللافلزات، خواص وسطى (مثل السيليكون والجرمانيوم).
المجموعة 1 (الفلزات القلوية): لينة، نشطة جدًا، تتفاعل مع الماء.
المجموعة 2 (الفلزات القلوية الترابية): أقل نشاطًا من المجموعة 1، صلبة.
المجموعة 17 (الهالوجينات): لافلزات نشطة، تتحد مع الفلزات لتكوين أملاح.
المجموعة 18 (الغازات النبيلة): خاملة، مستقرة، لا تتفاعل بسهولة.
العناصر الانتقالية: مجموعات 3-12، معظمها فلزات صلبة، ذات خواص مغناطيسية وتوصيلية جيدة.
إعداد المدرس: إيمان سلمان