الصف الثاني عشر المتقدم
كيمياء
الفصل الثالث
ملفات متنوعة
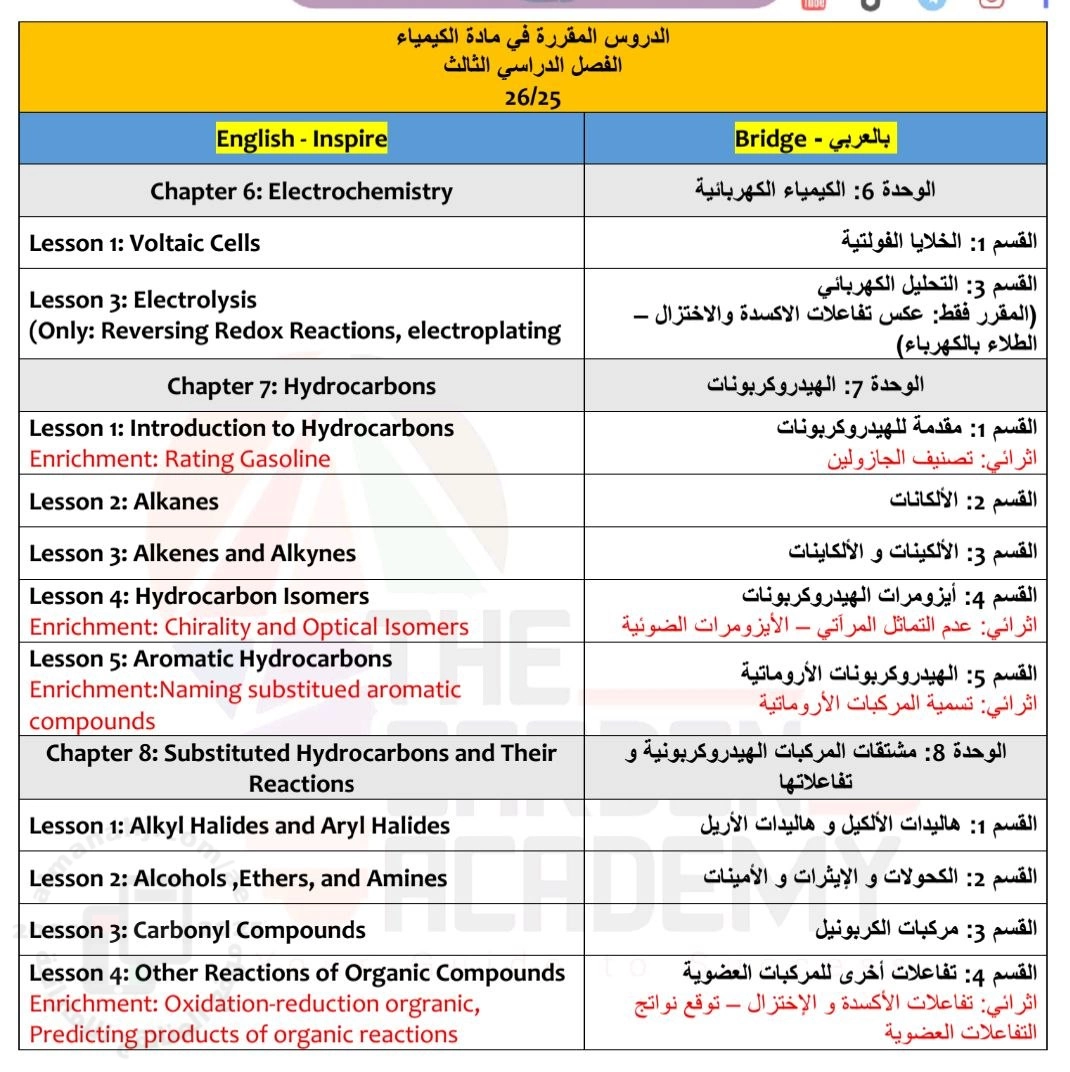
مقرر الوحدات والدروس المطلوبة في الفصل الثالث منهجي بريدج وانسباير
إعداد المدرّس: طارق محمد
2026-04-11 09:37
•2025-2026
•659.9KB
•👁 318